2026-03-16

摘要
《PLOS One》最新NPC小鼠模型研究评估了AAV9基因治疗的最佳干预时机与给药途径。详实的数据证实,早期(新生期)干预在延长生存期与减缓疾病进展方面具有决定性优势,且脑室注射(ICV)与早期静脉给药(FV)均展现出对小脑浦肯野细胞极强的挽救能力。
尼曼-匹克氏症C型(Niemann-Pick disease, type C,简称NPC)是一种罕见且致命的遗传性神经退行性疾病,在美国的活产婴儿中发病率约为十万分之一。大约95%的NPC患者是由NPC1基因突变引起的,该突变会导致溶酶体胆固醇输出受损。这种疾病会引发进行性的神经退行性病变,尤其是导致小脑浦肯野细胞(Purkinje cells)大量死亡,同时患者还会出现脾脏和肝脏的周围性疾病。
过去的研究已经证明,通过腺相关病毒(AAV)将NPC1基因递送至中枢神经系统(CNS),可以大幅延长缺乏Npc1基因小鼠的寿命,并减轻疾病症状。然而,为了找到临床疗效最大化的方案,科学家们需要确定:系统性静脉给药与直接脑室内给药相比,效果有何差异?新生期干预与断奶期干预相比,获益能提升多少?
2026年3月11日,国际学术期刊《PLOS One》发表了一项重要的对照研究。该研究首次直接平行比较了不同干预时期和递送途径对AAV9治疗NPC小鼠效果的定量与定性影响。
实验设计:控制变量,精准对比
为探究最佳参数,研究人员利用携带人类NPC1(hNPC1)基因的AAV9载体,对Npc1缺失小鼠进行了三组核心干预。实验设计涵盖了不同的时间窗口与注射路径,并在剂量上参考了各自途径的临床常规标准:
RO组(断奶期系统给药):在小鼠出生后31-34天,通过眶后静脉(Retro-orbital)注射,总剂量为1.21×1012基因组拷贝(GC)。
FV组(新生期系统给药):在小鼠出生后第1天,通过面静脉(Facial vein)注射,总剂量为1.0×1011GC。此剂量约为RO组的十分之一。
ICV组(新生期脑室给药):在小鼠出生后第1天,向右侧脑室注射(Intracerebroventricular),总剂量极低,仅为1.0×1010GC。此剂量约为RO组的百分之一。
此外,研究还平行对比了两种不同的启动子:截短的泛表达伸长因子-1α启动子(EF1a(s))与小鼠Mecp2衍生的神经特异性启动子(546启动子)。
核心数据解读
载体体内分布:新生期静脉注射可实现极高的“入脑率”
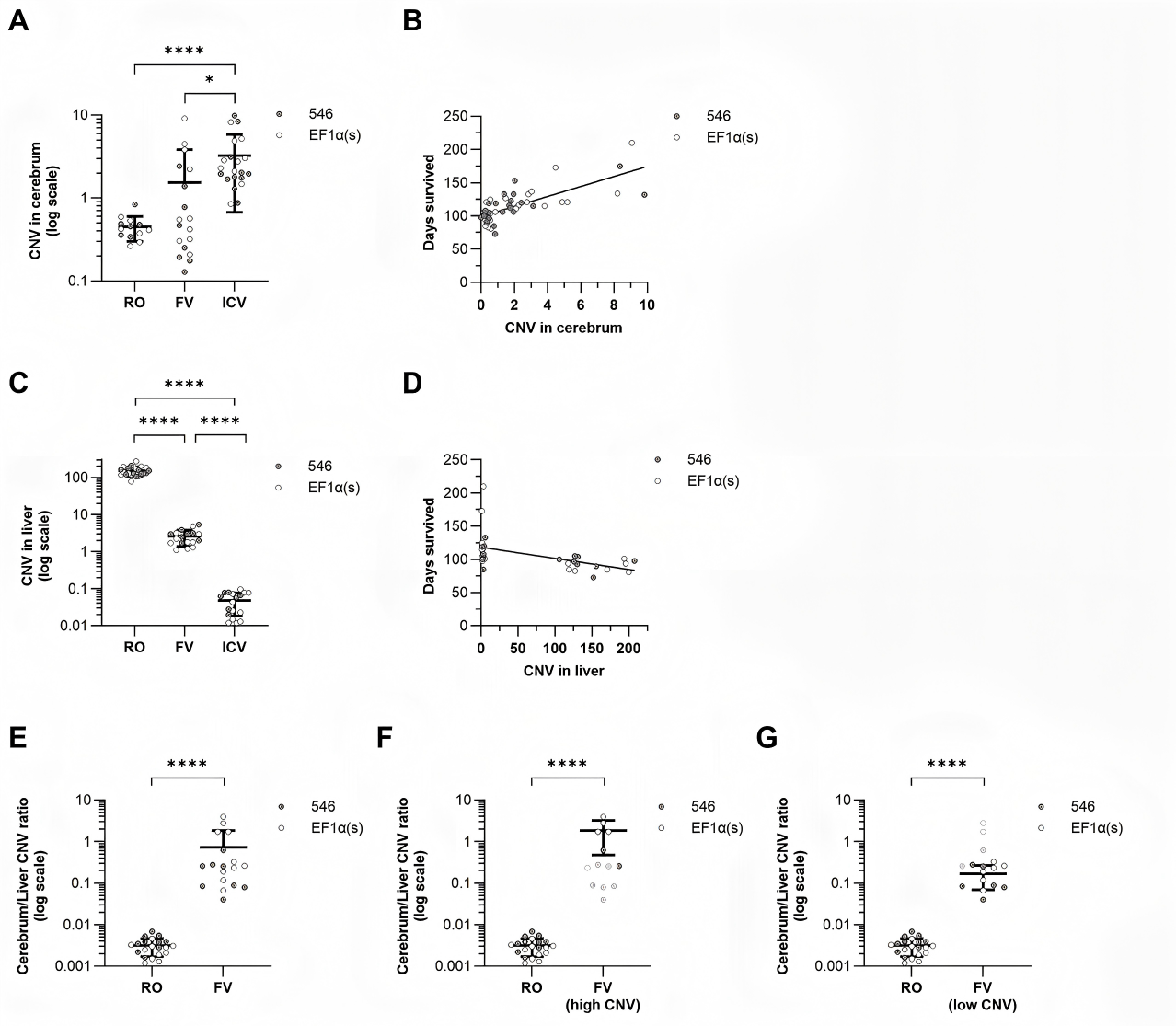
图1 大脑拷贝数与生存率提升呈正相关,且在新生鼠全身给药模型中,终末期大脑与肝脏的拷贝数比值显著高于断奶期小鼠模型
基因治疗能否逆转神经退行性病变,很大程度上取决于有多少有效载体能跨越血脑屏障进入大脑。研究团队通过ddPCR对小鼠终末期组织进行了定量分析。
大脑靶向效率(Fig 1A):直接注射到脑室的ICV组大脑拷贝数最高(3.3±2.6),显著高于新生期静脉注射的FV组(1.5±2.3)和断奶期静脉注射的RO组(0.4±0.2)。
肝脏富集情况(Fig 1C):断奶期RO组的载体大量富集在肝脏,其肝脏拷贝数(152.5±43.62)比FV组(2.6±1.21)高出40至70倍,比ICV组(0.048±0.029)高出3000多倍。
分布比例的惊人差异(Fig 1E):大脑与肝脏拷贝数比值是衡量靶向效率的关键。新生期FV组的该比值(0.73±1.1),总体上比断奶期RO组(0.0032±0.0015)高出了200多倍。这表明,如果在新生期进行静脉注射,由于血脑屏障等发育因素,AAV9能将更大比例的载体输送到大脑。
生存期的显著跃升:早期治疗具有决定性优势
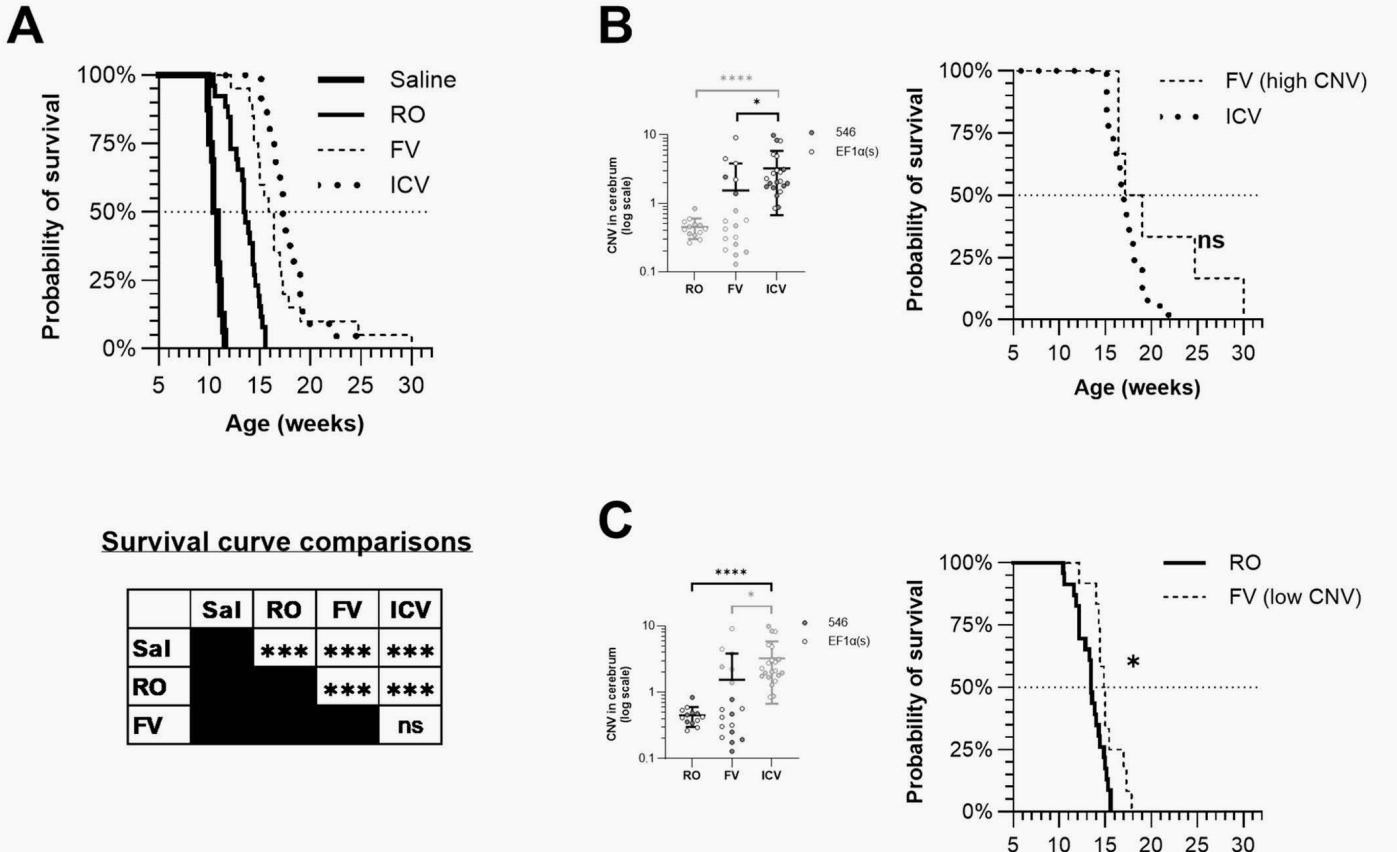
图2 AAV-hNPC1早期治疗通过大脑拷贝数变异(CNV)机制改善生存率
所有接受AAV治疗的组别,其中位生存率均显著高于未治疗的组别。
中位生存期对比(Fig 2A):未经治疗的生理盐水(Saline)对照组中位生存期仅为10.6周。断奶期给药的RO组提升至13.5周。而新生期给药的FV组和ICV组,中位生存期分别大幅跃升至16.1周和17.3周。
拷贝数与生存期的关联(Fig 2B, 2C):大脑中的载体拷贝数与存活时间呈现极显著的正相关(r=0.73)。尤其值得注意的是,即使在FV组中大脑拷贝数较低(类似于RO组)的亚群,其中位生存期(14.9周)也显著长于RO组(13.4周)。这进一步证实,早期干预本身就是延长寿命的独立且关键的因素。
逆转体重衰退:早治疗能重塑生长曲线
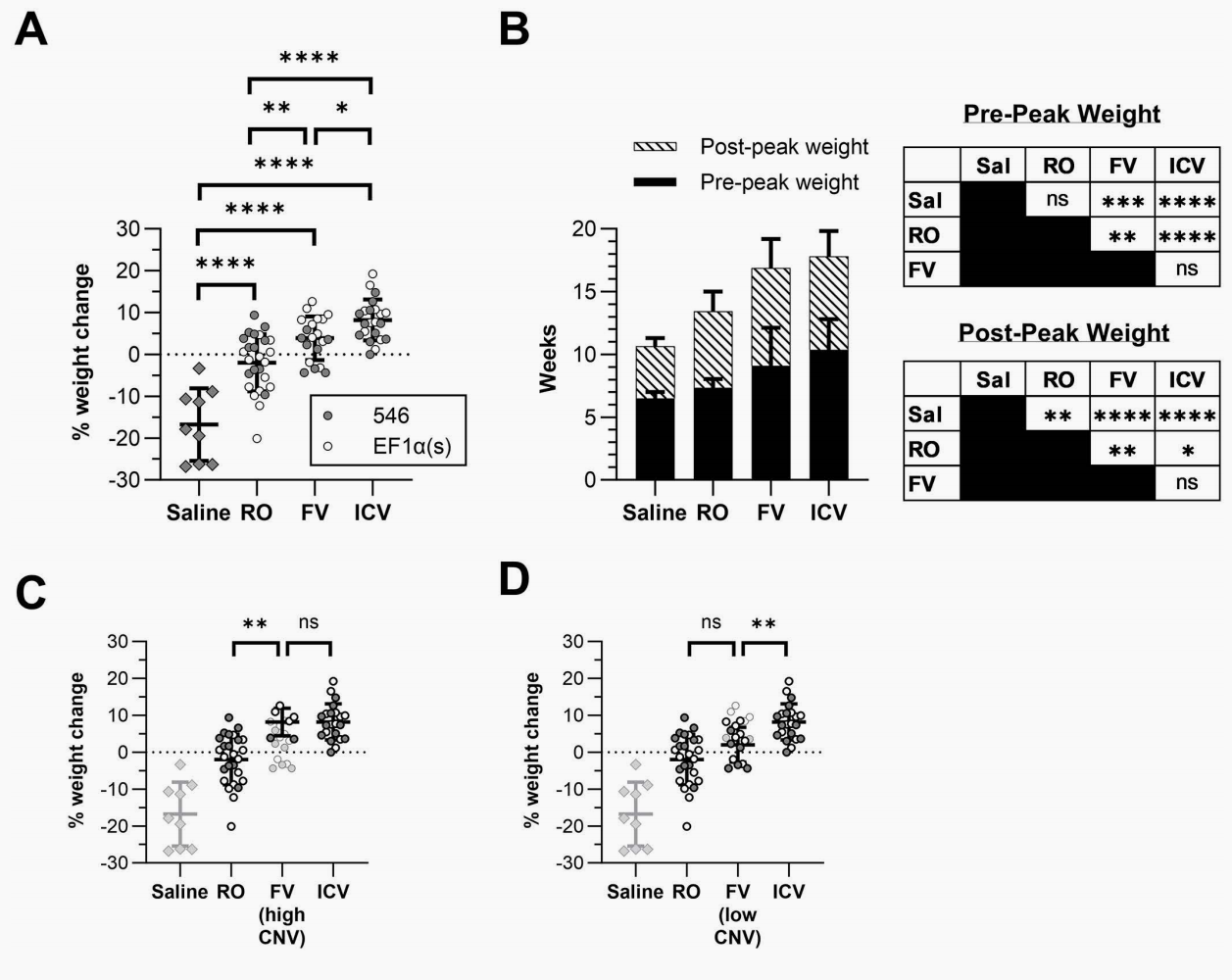
图3 AAV-hNPC1治疗可延长体重开始下降的时间并减缓体重下降速率
NPC小鼠病程恶化的核心指标之一,是在到达生长顶峰后出现不可逆的体重下降。
9周龄体重变化率(Fig 3A):在9周龄时,未治疗的对照组体重较6周龄时平均严重下降了16.8%±8.7%。断奶期的RO组将下降幅度控制在微降2.0%±6.8%。而新生期的FV组和ICV组则完全逆转了病理进程,体重分别保持了3.9%±5.2%和8.2%±4.9%的正向增长。
延长“正常生长期”(Fig 3B):对照组在平均6.5±0.5周龄时即达到峰值体重并开始衰退。而新生期干预不仅延缓了下降速度,还分别显著增加了到达峰值体重的时间(FV组推迟至9.1±3.0周,ICV组推迟至10.3±2.4周),为小鼠赢得了更长的正常生长期。
彻底的运动功能挽救:从步履蹒跚到行动自如
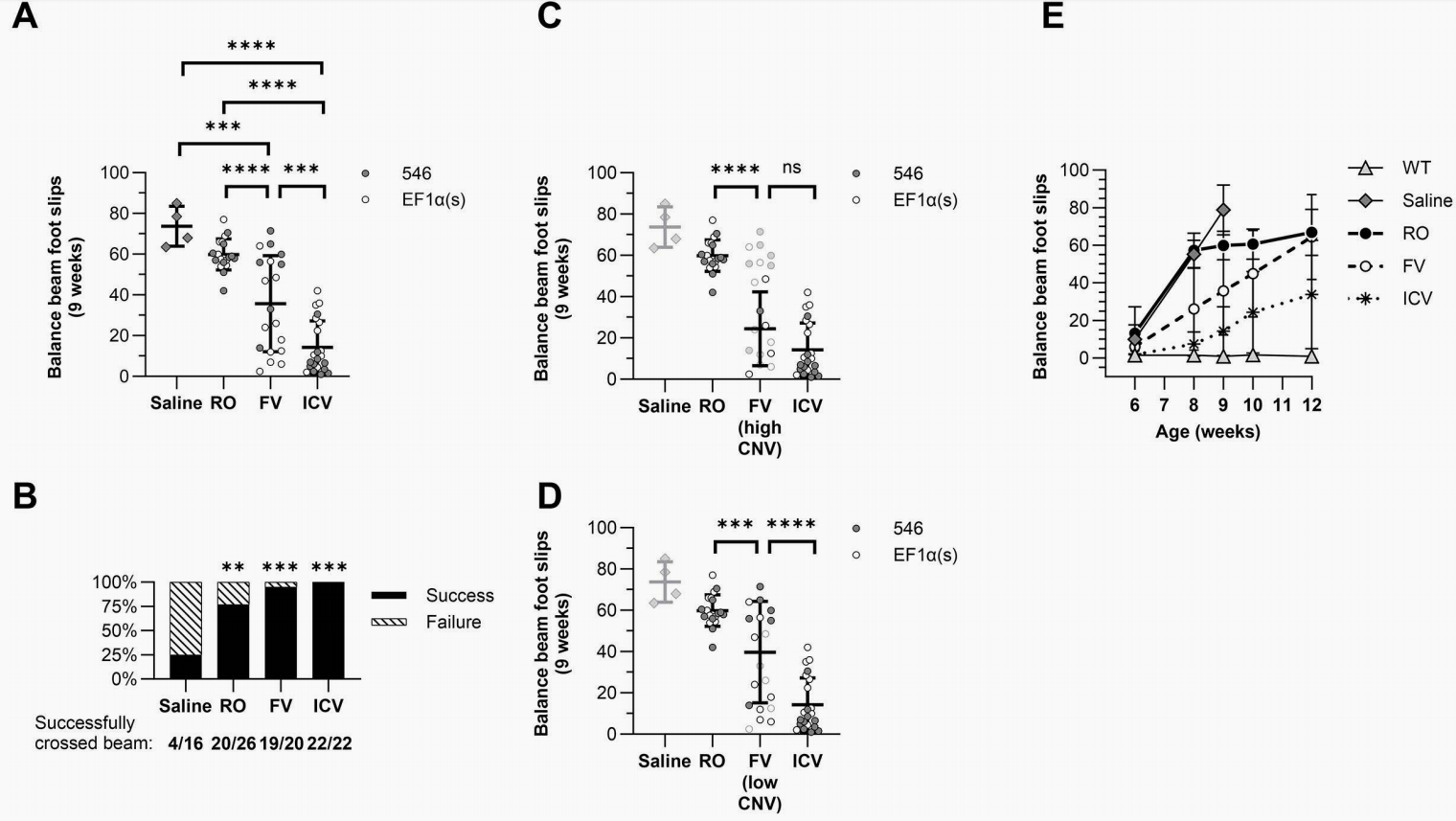
图5 AAV-hNPC1治疗在最早接受治疗的群体中对运动协调能力的影响最为显著
随着小脑功能的丧失,NPC小鼠会表现出严重的共济失调。研究采用了平衡木测试来客观量化小鼠的运动协调能力。
通过成功率(Fig 5B):在9周龄测试中,对照组仅有25%能成功穿过平衡木。治疗组的成功率大幅提升:RO组为77%,FV组为95%,ICV组达到了完美的100%。
失误滑落次数(Fig 5A):在成功通过平衡木的小鼠中,对照组平均失误高达73.8±9.8次。断奶期RO组降为59.8±7.6次。而新生期组别展现了压倒性优势:FV组降至35.7±23.5次,脑室注射的ICV组仅有14.3±13.0次失误。
细胞级病理学保护:拯救小脑浦肯野细胞
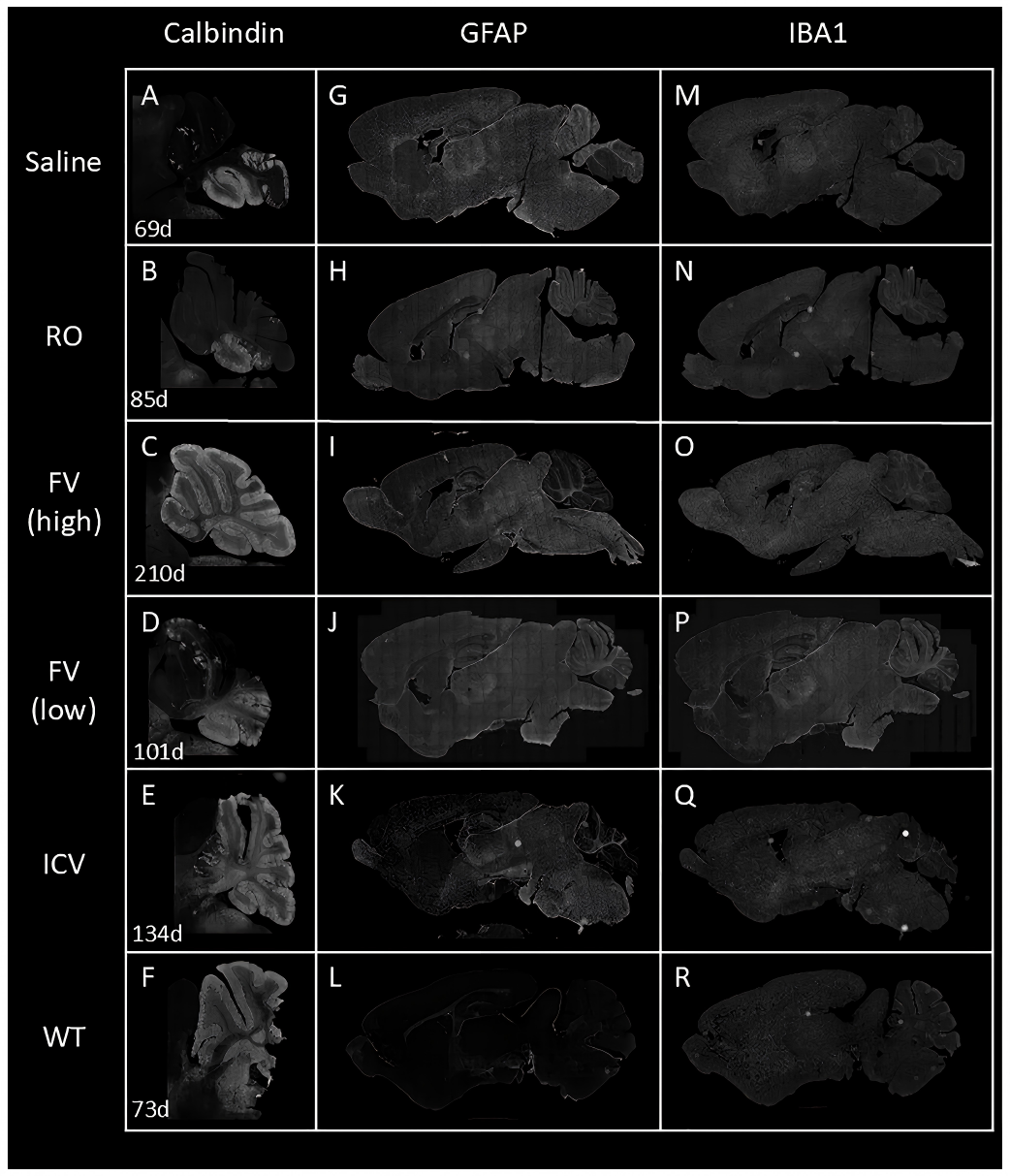
图6 AAV9-EF1α(s)-hNPC1治疗在终末期治疗组小鼠中保护浦肯野细胞并减轻中枢神经系统病理损伤
为了探寻行为学改善的生物学基础,研究团队对终末期小鼠的脑组织切片进行了抗Calbindin免疫荧光染色(标记浦肯野细胞)以及抗GFAP染色(标记神经炎症)。
浦肯野细胞的存留(Fig 6A-E):对照组和RO组小鼠到生命后期,小脑中的浦肯野细胞几乎凋亡殆尽,仅在后叶有极少量存活。然而,新生期ICV组小鼠呈现出一致且近乎完全的浦肯野细胞保留。同样具有突破意义的是,在新生期静脉注射(FV组)中吸收药物较好的小鼠,也实现了近乎完美的浦肯野细胞保护。
神经炎症的消退(Fig 6G-L):抗GFAP染色证实,ICV干预显著减少了大脑皮层、小脑等多个区域的星形胶质细胞增生(Astrocytosis),有效缓解了CNS的病理进程。
关于启动子的客观发现
在评估广泛表达的EF1a(s)启动子与神经元特异性的546启动子时,研究数据表明:两者在脑部和肝脏的载体拷贝数、生存期延长、体重变化百分比、综合疾病表型得分以及平衡木失误次数上,均未表现出统计学上的显著差异。这提示,在当前模型中,给药途径与时机对最终疗效的决定性作用,远大于这两种启动子之间的细微差别。
科学总结与现实考量
“早期干预”是疗效跃升的基础:相比于断奶期(相当于较晚确诊阶段),新生期的基因治疗在延长寿命、重塑生长曲线和阻断运动障碍方面具有无可比拟的优势。这强烈支持了在临床端推进罕见病早期基因筛查的必要性。
ICV递送具有极致的靶向效能:新生期直接脑室注射(ICV)以最低的绝对剂量(仅为常规系统性给药的百分之一),实现了最高的大脑靶向效率和最彻底的神经元保护。
极早期系统给药(静脉注射)的巨大潜力:研究首次明确证实,如果在生命极早期(血脑屏障尚未完全发育成熟时)进行静脉注射,AAV9能以极高比例穿透进入大脑,达到可媲美脑室内给药的浦肯野细胞挽救效果。此外,系统性给药能同时兼顾肝脏等外周脏器的治疗,这可能是进一步延长患者生存期的重要拼图。
晚期干预的现实意义:作者在讨论中客观指出,由于现实中新生儿筛查尚未普及,断奶期的静脉注射(RO)依然能够在多个客观指标上提供切实的临
床获益,这为错过极早期诊断的儿童患者提供了重要的治疗依据。
未来的突破方向,将有赖于具有更强中枢神经系统转导能力和血脑屏障穿透能力的新型工程化AAV衣壳的研发,以期在兼顾系统性给药便利性的同时,克服大年龄段患者入脑难的瓶颈 。

地址:中国武汉东湖高新区光谷七路128号 市场:17720522078 人事行政:027-62439686 邮箱:marketing@genevoyager.com
BD 商务总台:17720514121 /13886000399(BD 经理) /17720515371(BD 经理)
本公司所有产品仅供实验科研使用,不用于人体疾病治疗及临床诊断。